Alcani: structură, nomenclatură, izomerie. Izomeria alcanilor Alcanii sunt exemple de izomeri
În chimie, alcanii sunt hidrocarburi saturate în care lanțul de carbon este deschis și constă din carbon legat între ei prin legături simple. O altă trăsătură caracteristică a alcanilor este că nu conțin deloc legături duble sau triple. Uneori, alcanii sunt numiți parafine; faptul este că parafinele sunt de fapt un amestec de carboni saturați, adică alcani.
Formula alcanilor
Formula alcanului poate fi scrisă astfel:
În acest caz, n este mai mare sau egal cu 1.
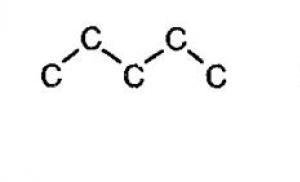
Alcanii sunt caracterizați de izomeria scheletului de carbon. În acest caz, conexiunile pot lua diferite forme geometrice, așa cum se arată de exemplu în imaginea de mai jos.

Izomeria scheletului de carbon al alcanilor
Pe măsură ce lanțul de carbon crește, crește și numărul de izomeri. De exemplu, butanul are doi izomeri.

Prepararea alcanilor
Alcanul este obținut de obicei prin diferite metode de sinteză. De exemplu, una dintre metodele de producere a unui alcan implică o reacție de „hidrogenare”, când alcanii sunt produși din carbohidrați nesaturați sub influența unui catalizator și la temperatură.
Proprietățile fizice ale alcanilor
Alcanii diferă de alte substanțe prin lipsa lor completă de culoare și sunt, de asemenea, insolubili în apă. Punctul de topire al alcanilor crește odată cu creșterea greutății moleculare și a lungimii lanțului de hidrocarburi. Adică, cu cât un alcan este mai ramificat, cu atât temperatura lui de ardere și topire este mai mare. Alcanii gazoși ard cu o flacără albastru pal sau incolor, în timp ce eliberează multă căldură.
Proprietățile chimice ale alcanilor
Alcanii sunt substanțe inactive din punct de vedere chimic, datorită rezistenței legăturilor sigma puternice C-C și C-H. În acest caz, legăturile C-C sunt nepolare, iar legăturile C-H sunt polare scăzute. Și deoarece toate acestea sunt tipuri de legături cu polarizare scăzută care aparțin tipului sigma, ele vor fi rupte conform unui mecanism omolitic, în urma căruia se formează radicali. Și, în consecință, proprietățile chimice ale alcanilor sunt în principal reacții de substituție radicală.
Aceasta este formula pentru substituția radicală a alcanilor (halogenarea alcanilor).
În plus, se pot distinge și reacții chimice precum nitrarea alcanilor (reacția Konovalov).
Această reacție are loc la o temperatură de 140 C și este cel mai bine cu un atom de carbon terțiar.
Cracarea alcanilor - această reacție are loc sub acțiunea temperaturilor ridicate și a catalizatorilor. Apoi sunt create condiții când alcanii superiori își pot rupe legăturile pentru a forma alcani de ordin inferior.
Alcanii sunt hidrocarburi saturate în moleculele cărora toți atomii de carbon sunt ocupați prin legături simple de către atomi de hidrogen. Prin urmare, omologii seriei metanului sunt caracterizați de izomeria structurală a alcanilor.
Izomeria scheletului de carbon
Omologii cu patru sau mai mulți atomi de carbon sunt caracterizați de izomerie structurală datorită modificărilor scheletului de carbon. Grupările metil -CH 2 se pot atașa la orice carbon al lanțului, formând noi substanțe. Cu cât sunt mai mulți atomi de carbon în lanț, cu atât se pot forma mai mulți izomeri omologi. Numărul teoretic de omologi se calculează matematic.

Orez. 1. Numărul aproximativ de izomeri ai omologilor metanului.
Pe lângă grupările metil, lanțurile lungi de carbon pot fi atașate de atomii de carbon, formând substanțe complexe ramificate.
Exemple de izomerie a alcanilor:
- butan normal sau n-butan (CH3-CH2-CH2-CH3) şi 2-metilpropan (CH3-CH(CH3)-CH3);
- n-pentan (CH3-CH2-CH2-CH2-CH3), 2-metilbutan (CH3-CH2-CH(CH3)-CH3), 2,2-dimetilpropan (CH3-C (CH3)2-CH3);
- n-hexan (CH3-CH2-CH2-CH2-CH2-CH3), 2-metilpentan (CH3-CH(CH3)-CH2-CH2-CH3), 3-metilpentan ( CH3-CH2-CH(CH3)-CH2-CH3), 2,3-dimetilbutan (CH3-CH(CH3)-CH(CH3)-CH3), 2,2-dimetilbutan ( CH3-C(CH3)2-CH2-CH3).

Orez. 2. Exemple de izomeri structurali.
Izomerii ramificati diferă de moleculele liniare prin proprietăți fizice. Alcanii ramificati se topesc și fierb la temperaturi mai scăzute decât omologii lor liniari.
Nomenclatură
Nomenclatura internațională IUPAC a stabilit reguli pentru denumirea lanțurilor ramificate. Pentru a numi un izomer structural:
- găsiți cel mai lung lanț și numiți-l;
- numerotați atomii de carbon începând de la capătul cu cei mai mulți substituenți;
- indicați numărul de substituenți identici folosind prefixe numerice;
- dați nume înlocuitorilor.
Numele este format din patru părți, care se succed:
- numere care indică atomii lanțului care au substituenți;
- prefixe numerice;
- numele deputatului;
- numele circuitului principal.
De exemplu, în molecula CH3-CH(CH3)-CH2-C(CH3)2-CH3, catena principală are cinci atomi de carbon. Deci este pentan. Capătul drept are mai multe ramuri, așa că numerotarea atomilor începe de aici. În acest caz, al doilea atom are doi substituenți identici, ceea ce se reflectă și în nume. Se pare că această substanță se numește 2,2,4-trimetilpentan.
Diferiții substituenți (metil, etil, propil) sunt enumerați în nume alfabetic: 4,4-dimetil-3-etilheptan, 3-metil-3-etiloctan.
De obicei, se folosesc prefixe numerice de la doi la patru: di- (doi), tri- (trei), tetra- (patru).
Ce am învățat?
Alcanii sunt caracterizați prin izomerie structurală. Izomerii structurali sunt caracteristici tuturor omologilor, începând cu butan. În izomeria structurală, substituenții se atașează la atomii de carbon din lanțul de carbon, formând lanțuri ramificate complexe. Numele izomerului constă din numele catenei principale, substituenți, o desemnare verbală a numărului de substituenți și o denumire digitală a atomilor de carbon la care sunt atașați substituenții.
Data de: ____________
11-11
Alcani. Serii omoloage de alcani. Nomenclatura și izomeria alcanilor
SUBIECT
ŢINTĂ
Pentru a oferi studenților conceptul de hidrocarburi saturate, structura lor chimică, spațială și electronică. Pentru a vă familiariza cu conceptul de omologie, regulile de denumire a substanțelor și de redactare a formulelor conform nomenclaturii moderne. Continuați formarea conceptelor ideologice: despre cunoașterea naturii, relația cauză-efect dintre compoziția, structură, proprietăți și utilizarea hidrocarburilor saturate.
CONŢINUT
Serii omoloage de alcani și structura lor
TERMENI
Alcan, omologi, izomeri
EXPERIMENT CHIM
ECHIPAMENTE
tabla interactiva
SARCINA CASĂ
PLANUL LECȚIEI.
Sondaj pentru teme. Actualizarea cunoștințelor
Alcani. (Hidrocarburi saturate. Parafine. Hidrocarburi saturate.)
Alcanii sunt hidrocarburi în molecule în care toți atomii de carbon sunt legați prin legături simple (-) și au formula generală:
C n H 2n+2
Ce sunt omologii? (elevii răspund la această întrebare)
Serii omoloage de alcani
Alcani, având formula generală C n H 2 n +2 , sunt o serie de compuși înrudiți cu același tip de structură, în care fiecare membru ulterior diferă de cel anterior printr-un grup constant de atomi (-CH 2 -). Această secvență de conexiuni se numeșteserie omoloagă (din greaca omolog - similar), membri individuali ai acestei serii -omologi , iar grupul de atomi în care se deosebesc omologii vecini estediferenta omologica .
Seria omoloagă de alcani poate fi compilată cu ușurință prin adăugarea de fiecare dată a unui nou atom de carbon la lanțul anterior și suplimentând valențele sale rămase cu până la 4 atomi de hidrogen. O altă opțiune este adăugarea unui grup -CH la lanț 2 -:
CH 4 sau N-CH 2 -H – primul membru al seriei omoloage –metan
(conține 1 atom de carbon);
CH 3 - CH 3 sau N-CH 2 -CH 2 -H – al doilea omolog –etan (2 atomi de C);
CH 3 - CH 2 - CH 3 sau N-CH 2 -CH 2 -CH 2 -H – al treilea omolog –propan (3 atomi de C);
CH 3 - CH 2 - CH 2 - CH 3 sau N-CH 2 -CH 2 -CH 2 - CH 2 - N –butan (4 atomi de C)
Sufix-un este caracteristica denumirilor tuturor alcanilor. Pornind de la al cincilea omolog, denumirea alcanului se formează din cifra grecească, indicând numărul de atomi de carbon din moleculă și sufixul-un : pentan C 5 N 12 , hexan C 6 N 14 , heptan C 7 N 16 , octan C 8 N 18 , nonane C 9 N 20 , Dean C 10 N 22 etc.
Tipuri de izomerie pentru alcani:
Izomeria este fenomenul de existență a unor compuși care au aceeași compoziție (aceeași formulă moleculară), dar structuri diferite. Se numesc astfel de conexiuniizomerii .
Diferențele în ordinea în care atomii sunt combinați în molecule (adică structura chimică) duc laizomerie structurală . Structura izomerilor structurali este reflectată de formulele structurale. În seria alcanilor, izomeria structurală apare atunci când lanțul conține 4 sau mai mulți atomi de carbon, adică începând cu butanul C. 4 N 10 . Dacă în molecule cu aceeași compoziție și aceeași structură chimică sunt posibile poziții relative diferite ale atomilor în spațiu, atunci observămizomerie spațială (stereoizomerie) . În acest caz, utilizarea formulelor structurale nu este suficientă și ar trebui folosite modele moleculare sau formule spațiale (stereochimice). Alcani, începând cu etan C 2 N 6 , există în diferite forme spațiale datorită rotației intramoleculare de-a lungul legăturilor C-C s și prezintă așa-numitaizomerie rotațională .
În plus, dacă există 7 sau mai mulți atomi de carbon într-o moleculă, este posibil un alt tip de izomerie spațială, atunci când doi izomeri se relaționează unul cu celălalt ca obiect și imaginea în oglindă (similar cu modul în care mâna stângă se raportează la dreapta).
Astfel de diferențe în structura moleculelor sunt numiteoglindă sauoptic izomerie.
Algoritm.
1. Selectarea circuitului principal:

2. Numerotarea atomilor din lanțul principal:

3. Formarea numelui:

2 - metilbutan
Structura alcanilor.
Atomul de carbon din toate substanțele organice este într-o stare „excitată”, adică are patru electroni nepereche la nivelul exterior.
Fiecare nor de electroni are o rezervă de energie: norul s are o rezervă mai mică de energie decât norul p; în atomul de carbon se află în stări energetice diferite. Prin urmare, atunci când se formează o legătură chimică, are loc hibridizarea, adică alinierea norilor de electroni în ceea ce privește rezerva de energie. Acest lucru se reflectă în forma și direcția norilor; are loc o restructurare (spațială) a norilor de electroni.
Ca urmare a hibridizării sp3, toți cei patru nori de electroni de valență sunt hibridizați: unghiul de legătură dintre aceste axe ale norilor hibridizați este de 109° 28", prin urmare moleculele au o formă tetraedrică spațială, forma lanțurilor de carbon este în zig-zag; atomii de carbon nu sunt pe aceeași linie dreaptă, deoarece în timpul rotației atomii unghiurile de legătură rămân aceleași.
Toate substanțele organice sunt construite în principal prin legături covalente. Legăturile carbon-carbon și carbon-hidrogen sunt denumite legături sigma - o legătură formată atunci când orbitalii atomici se suprapun de-a lungul unei linii care trece prin nucleele atomice. Rotația în jurul legăturilor sigma este posibilă, deoarece această legătură are simetrie axială.
Pentru a consolida materialul, răspundeți la întrebările de la sfârșitul paragrafului, precum și finalizați sarcinile din cartea de probleme
Teme pentru acasă: §3.1 repovestire, Nr. 3,4,6,8 p. 67
Scop: familiarizarea studenților cu caracteristicile structurale, seriile omoloage, izomeria, nomenclatura alcanilor și prepararea acestora.
- Educational. Obțineți o înțelegere inițială a alcanilor (formula generală, seria omoloagă de alcani, compoziția și structura lor, aplicații).
- De dezvoltare. Dezvoltați înțelegerea timpurie a izomeriei și capacitatea de a da nume folosind nomenclatura IUPAC.
- Educational. Să cultive dorința de a învăța activ, cu interes, pentru a crește motivația de a studia chimia.
Dotare: calculator, proiector multimedia, ecran.
Progresul lucrărilor
I. Moment organizatoric.
II. Blocul motivațional.
Profesor. Continuăm să studiem chimia organică. Te invit să călătorești cu 160 de ani înapoi în Anglia bună (Prezentare.Slide 1) .
1848 Hannah Greener, în vârstă de 15 ani, a murit la Newcastle în timpul unei intervenții chirurgicale minore. Doctorul Meggison, cel care a efectuat operația, a declarat faptele după cum urmează în timpul anchetei. „Am așezat pacienta pe un scaun și i-am adus la nas o batistă umezită cu doar o linguriță din această substanță. Hannah a tras două respirații. După un minut, i-am cerut asistentului meu să înceapă operația. După încă un minut, i-am deschis puțin ochii, au rămas deschiși, vasele sclerei erau pline de sânge, buzele și fața i-au devenit foarte albe. Am decis să fac sângerări din vene, dar nu am primit mai mult de o lingură de sânge. Cred că era moartă înainte de încercarea mea de a vărsa sânge. Nu au trecut mai mult de trei minute din momentul primei inhalări a acestei substanțe și până la moarte.” Ceea ce a cauzat moartea lui Hannah este încă un mister. Despre ce substanță crezi că vorbim? ( Toate sugestiile sunt ascultate.) Cloroform. Găsiți formula. (Folosiți o carte de referință, internetul.)CH3CI. Această substanță este un derivat al CH4. Cărei clase aparține această substanță? Alcani.(Elevii notează subiectul lecției în caiete.) Alcanii, prima clasă din toate clasele de substanțe organice pe care le vom studia. Prin urmare, vă propun un plan conform căruia vor fi studiate toate clasele de substanțe organice.
1. Definiție. Formulă. Compus.
2. Structura.
3. Serii omoloage. Nomenclatură.
4. Tipuri de izomerie.
5. Metode de obţinere.
6. Proprietăți fizice.
7. Proprietăți chimice.
8. Aplicare.
(Punctele 1–5 sunt studiate în prima lecție, 6–8 în a doua lecție.)
III. Stabilirea obiectivelor.
Privește primele 5 puncte ale planului și formulează scopul lecției.
IV. Efectuarea blocului.
Profesor: Ce părere aveți, de ce trebuie să studiem alcanii? Deschide manualul p.79. luați în considerare schema de utilizare a alcanilor. După cum puteți vedea, alcanii au o gamă largă de utilizări. Prin urmare, cred că fiecare persoană ar trebui să știe despre structura, proprietățile și producția acestor substanțe.
Profesor. Ce știi despre alcani? (Toate răspunsurile elevilor sunt scrise pe tablă. Formula generală CnH2n+2; C-C legătură simplă, -an) Pe baza notelor, elevii oferă o descriere generală a alcanilor. Verificați diapozitivul (Diapozitivul 2).
Dintre formulele substanțelor organice, alegeți formulele alcanilor ( lucrul cu simulatorul) (Anexa 1). Profesorul scrie pe tablă toate formulele găsite de elevi într-o coloană. Se formează un număr de substanțe care diferă unele de altele prin una sau mai multe grupe CH2. Elevii concluzionează că s-a format o serie omologică (Diapozitivul 3).
Amintiți-vă de nomenclatura alcanilor.
Profesor. Studiem structura alcanilor folosind exemplul unei molecule de metan . După vizualizarea fragmentului răspunde la întrebările: – Ce este hibridizarea ? – Ce tip de hibridizare au alcanii? – Unghiurile dintre orbiti? Lungimea C-Link-ului? (vizualizați Structura moleculei de metan (N 132051) TsOR). (Lucreaza cu Slide 4).
Profesor. Să ne amintim ce este izomeria și ce tipuri de izomerie sunt caracteristice substanțelor organice (Diapozitivul 5).
Ce tipuri de izomerie credeți că sunt caracteristice apcanilor? Prin metoda eliminării, elevii stabilesc că alcanii sunt caracterizați printr-un tip de izomerie. Izomeria scheletului de carbon. Unul dintre elevi vine la tablă pentru a construi izomeri pentru o substanță cu formula C5H12, le dă nume folosind nomenclatura IUPAC (se nota). Dacă se dorește, un student este invitat la tablă pentru a finaliza sarcina inversă.
Exercițiu. Alcătuiți formule structurale pentru următoarele substanțe.
a) 2,3 dimetilpentan; b) 2,5 dimetilhexan; d) 3 metil-3 etilheptan (Primește o notă).
Profesor. Deoarece alcanii sunt utilizați pe scară largă, este necesar să se studieze metodele de preparare a acestora . (Recepția este studiată folosind manualul p. 70. Reacțiile sunt notate într-un caiet din Slide 6)
V. Bloc de control și evaluare.
Este oferită muncă independentă sub formă de test (Anexa 2). (Există verificare reciprocă și se acordă note). Reveniți la planul lecției, uitați-vă la 1–5 puncte, răspundeți la întrebări
– Ne-am atins scopul?
– Ce nou ai învățat la lecție?
– Ce a fost interesant?
ALCANE (hidrocarburi saturate, parafine)
- Alcanii sunt hidrocarburi saturate alifatice (aciclice) în care atomii de carbon sunt legați între ei prin legături simple (single) în lanțuri drepte sau ramificate.
Alcani– denumirea hidrocarburilor saturate conform nomenclaturii internaționale.
Parafine– un nume stabilit istoric care reflectă proprietățile acestor compuși (din lat. parrum affinis– având afinitate mică, activitate scăzută).
Limită, sau saturate, aceste hidrocarburi sunt denumite datorită saturației complete a lanțului de carbon cu atomi de hidrogen.
Cei mai simpli reprezentanți ai alcanilor:
Modele de molecule:


Când comparăm acești compuși, este clar că ei diferă unul de celălalt printr-un grup -CH2 - (metilen). Adăugarea unui alt grup la propan -CH2 -, primim butan C4H10, apoi alcani C5H12, C6H14 etc.
Acum putem deriva formula generală a alcanilor. Se consideră că numărul de atomi de carbon din seria alcanilor este n
, atunci numărul de atomi de hidrogen va fi 2n+2
. Prin urmare, compoziția alcanilor corespunde formulei generale CnH2n+2.
Prin urmare, este adesea folosită următoarea definiție:
Alcani- hidrocarburi, a căror compoziție este exprimată prin formula generală CnH2n+2, Unde n – numărul de atomi de carbon.
Structura alcanilor
Structura chimică(ordinea de conectare a atomilor din molecule) a celor mai simpli alcani - metan, etan si propan - este prezentata prin formulele lor structurale date in sectiunea 2. Din aceste formule reiese clar ca exista doua tipuri de legaturi chimice in alcani:
S–SȘi SH.
Legătura C-C este covalentă nepolară. Legătura C–H este covalentă, slab polară, deoarece carbonul și hidrogenul sunt apropiate ca electronegativitate (2,5 pentru carbon și 2,1 pentru hidrogen). Formarea legăturilor covalente în alcani datorită perechilor de electroni împărtășiți de atomi de carbon și hidrogen poate fi demonstrată folosind formule electronice:

Formulele electronice și structurale reflectă structura chimica, dar nu da o idee despre structura spațială a moleculelor, care afectează în mod semnificativ proprietățile substanței.
Structura spațială, adică aranjarea relativă a atomilor unei molecule în spațiu depinde de direcția orbitalilor atomici (AO) ai acestor atomi. În hidrocarburi, rolul principal îl joacă orientarea spațială a orbitalilor atomici ai carbonului, deoarece 1s-AO sferic al atomului de hidrogen îi lipsește o orientare specifică.
Aranjarea spațială a carbonului AO, la rândul său, depinde de tipul de hibridizare a acestuia (Partea I, Secțiunea 4.3). Atomul de carbon saturat din alcani este legat de alți patru atomi. Prin urmare, starea sa corespunde hibridizării sp 3 (Partea I, secțiunea 4.3.1). În acest caz, fiecare dintre cele patru AO de carbon hibrid sp 3 participă la suprapunerea axială (σ-) cu s-AO al hidrogenului sau cu sp 3 -AO al altui atom de carbon, formând legături σ-CH sau C-C.

Cele patru legături σ ale carbonului sunt direcționate în spațiu la un unghi de 109 aproximativ 28", ceea ce corespunde cu cea mai mică respingere a electronilor. Prin urmare, molecula celui mai simplu reprezentant al alcanilor - metanul CH4 - are forma unui tetraedru, în centrul căruia se află un atom de carbon, iar la vârfuri sunt atomi de hidrogen:

Unghiul de legătură H-C-H este de 109°28". Structura spațială a metanului poate fi prezentată folosind modele volumetrice (la scară) și modele cu bile și stick.
Pentru înregistrare, este convenabil să utilizați o formulă spațială (stereochimică).

În molecula următorului omolog - etan C 2 H 6 - două tetraedrice sp 3 atomi de carbon formează o structură spațială mai complexă:

Moleculele de alcan care conțin mai mult de 2 atomi de carbon se caracterizează prin forme curbate. Acest lucru poate fi arătat cu un exemplu n-butan (model VRML) sau n-pentan:

Izomeria alcanilor
- Izomeria este fenomenul de existență a unor compuși care au aceeași compoziție (aceeași formulă moleculară), dar structuri diferite. Se numesc astfel de conexiuni izomerii.
Diferențele în ordinea în care atomii sunt combinați în molecule (adică structura chimică) duc la izomerie structurală. Structura izomerilor structurali este reflectată de formulele structurale. În seria alcanilor, izomeria structurală se manifestă atunci când lanțul conține 4 sau mai mulți atomi de carbon, adică. începând cu butan C4H10.
Dacă în molecule cu aceeași compoziție și aceeași structură chimică sunt posibile poziții relative diferite ale atomilor în spațiu, atunci observăm izomerie spațială (stereoizomerie). În acest caz, utilizarea formulelor structurale nu este suficientă și ar trebui folosite modele moleculare sau formule speciale - stereochimice (spațiale) sau de proiecție.
Alcanii, începând cu etan H 3 C–CH 3, există în diferite forme spațiale ( conformaţiilor), cauzată de rotația intramoleculară de-a lungul legăturilor C–C σ și prezintă așa-numita izomerie rotațională (conformațională)..
În plus, dacă o moleculă conține un atom de carbon legat de 4 substituenți diferiți, este posibil un alt tip de izomerie spațială, atunci când doi stereoizomeri se relaționează unul cu celălalt ca obiect și imaginea în oglindă (similar cu modul în care mâna stângă se raportează la dreapta) . Astfel de diferențe în structura moleculelor sunt numite izomerie optică.
Izomeria structurală a alcanilor
- Izomerii structurali sunt compuși de aceeași compoziție care diferă în ordinea legăturii atomilor, adică. structura chimică a moleculelor.
Motivul manifestării izomeriei structurale în seria alcanilor este capacitatea atomilor de carbon de a forma lanțuri de structuri diferite.Acest tip de izomerie structurală se numește izomeria scheletului de carbon.
De exemplu, un alcan cu compoziţia C4H10 poate exista sub formă Două izomeri structurali:

şi alcan C5H12 - sub formă Trei izomeri structurali, care diferă în structura lanțului de carbon:

Odată cu creșterea numărului de atomi de carbon din molecule, crește posibilitățile de ramificare a lanțului, adică. numărul de izomeri crește odată cu numărul de atomi de carbon.

Izomerii structurali diferă în ceea ce privește proprietățile fizice. Alcanii cu structură ramificată, datorită împachetării mai puțin dense a moleculelor și, în consecință, a interacțiunilor intermoleculare mai mici, fierb la o temperatură mai scăzută decât izomerii lor neramificati.
La derivarea formulelor structurale ale izomerilor se folosesc următoarele tehnici.